Punjab State Board PSEB 10th Class Science Book Solutions Chapter 3 धातु एवं अधातु Textbook Exercise Questions, and Answers.
PSEB Solutions for Class 10 Science Chapter 3 धातु एवं अधातु
PSEB 10th Class Science Guide धातु एवं अधातु Textbook Questions and Answers
प्रश्न 1.
निम्नलिखित में से कौन-सा युगल विस्थापन अभिक्रिया प्रदर्शित करता है :
(a) NaCl विलयन एवं कॉपर धातु
(b) MgCl2 विलयन एवं ऐलुमीनियम धातु
(c) FeSO4 विलयन एवं सिल्वर धातु
(d) AgNO3 विलयन एवं कॉपर धातु।
उत्तर-
सिल्वर धातु से अधिक क्रियाशील होने के कारण, कॉपर धातु AgNO, के विलयन में से सिल्वर को अलग (विस्थापित) करने की क्षमता रखता है। इसलिए AgNO3 (aq) + Cu (s) → CuNO3 (aq) + Ag (s)
अन्य सभी धातुएँ दिए गए विलयन में उपस्थित धातु से कम अभिक्रियाशील हैं। इसलिए (d) युग्ल विस्थापन अभिक्रिया प्रदर्शित करता है।
प्रश्न 2.
लोहे के फ्राईंग पैन (Frying pan) को जंग से बचाने के लिए निम्न में से कौन-सी विधि उपयुक्त
(a) ग्रीज़ लगाकर
(b) पेंट लगाकर
(c) जिंक की परत चढ़ाकर
(d) ऊपर के सभी।
उत्तर-
(a) और (b) उपयुक्त नहीं है क्योंकि ग्रीज़ और पेंट दोनों ही गर्म करने पर जल जाते हैं। इसलिए (c) ज़िंक की परत लगाकर।
प्रश्न 3.
कोई धातु ऑक्सीजन के साथ अभिक्रिया कर उच्च गलनांक वाला यौगिक निर्मित करती है। यह यौगिक जल में विलेय है। यह तत्त्व क्या हो सकता है ?
(a) कैल्सियम
(b) कार्बन
(c) सिलिकन
(d) लोहा।
उत्तर-
कैल्सियम, ऑक्सीजन के साथ अभिक्रिया कर कैल्सियम ऑक्साइड बनाता है जो एक आयनिक यौगिक है। इसका गलनांक उच्च होता है तथा यह जल के साथ अभिक्रिया करने पर कैल्सियम हाइड्रोक्साइड बनाता है।
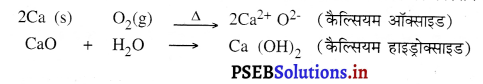
∴ ठीक उत्तर है (a) कैल्सियम।।
प्रश्न 4.
खाद्य पदार्थ के डिब्बों पर जिंक की बजाय टिन का लेप होता है क्योंकि
(a) टिन की अपेक्षा ज़िंक महँगा है।
(b) टिन की अपेक्षा जिंक का गलनांक अधिक है।
(c) टिन की अपेक्षा जिंक अधिक अभिक्रियाशील है।
(d) टिन की अपेक्षा जिंक कम अभिक्रियाशील है।
उत्तर-
टिन की अपेक्षा जिंक अधिक अभिक्रियाशील होता है तथा खाने में पाए जाने वाले तत्त्वों के साथ अभिक्रिया कर सकता है। इसलिए सही उत्तर है (c) टिन की अपेक्षा जिंक अधिक अभिक्रियाशील है।
प्रश्न 5.
आपको एक हथौड़ा, बैटरी, बल्ब, तार एवं स्विच दिया गया है :
(a) इनका उपयोग कर धातुओं एवं अधातुओं के नमूनों के बीच आप विभेद कैसे कर सकते हैं ?
(b) धातुओं एवं अधातुओं में विभेदन के लिए इन परीक्षणों की उपयोगिता का आकलन कीजिए।
उत्तर-
(a)
- हम धातुओं तथा अधातुओं के नमूनों को हथौड़े की सहायता से पीट-पीट कर पतली चादरों से परिवर्तित करने का प्रयास करेंगे।
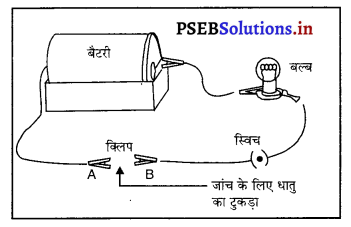
- बैटरी, बल्ब, तारों तथा स्विच की सहायता से हम एक विद्युत् परिपथ स्थापित करेंगे तथा धातु अथवा अधातु को परीक्षण के लिए उन्हें परिपथ के टर्मिनल A तथा B के बीच रखेंगे।
(b)
- यह पाया जाता है कि हथौड़े से पीटने पर धातुएँ पतली चादरों में परिवर्तित हो जाती हैं, जबकि अधातुएँ भंगुर होती हैं अर्थात्, हथौड़े से पीटने पर छोटेछोटे टुकड़ों में टूट जाती हैं। अतः धातुएँ आघातवर्ध्य होती हैं, जबकि अधातुएँ नहीं होतीं।
- दूसरे परीक्षण के दौरान यह पाया जाता है कि स्विच जब धातुएँ टर्मिनल A तथा B के बीच रखी जाती हैं तो A + B बल्ब जलने लगता है, जबकि अधातुओं को रखने पर जांच के लिए धातु बल्ब नहीं जलता। अतः धातुएँ विद्युत् की अच्छी चालक का टुकड़ा होती हैं, जबकि अधातुएँ विद्युत् की कुचालक होती हैं।
प्रश्न 6.
उभयधर्मी ऑक्साइड क्या होते हैं ? दो उभयधर्मी ऑक्साइडों का उदाहरण दीजिए।
उत्तर-
उभयधर्मी ऑक्साइड- जो धात्विक ऑक्साइड अम्लीय और क्षारीय दोनों प्रकार का व्यवहार प्रकट करते हैं, उन्हें उभयधर्मी ऑक्साइड कहते हैं।
उदाहरण-
(i) एल्यूमीनियम ऑक्साइड (Al2O3)
(ii) जिंक ऑक्साइड (ZnO).
(i) Al2O3 + 6HCl → 2AlCl3 + 3H2O (क्षारीय व्यवहार)
Al2O3 + 2NaOH → 2NaAlO2 + H2O (अम्लीय व्यवहार)
(ii) ZnO + 2HCl → ZnCl2 + H2O (क्षारीय व्यवहार)
ZnO + 2NaOH → Na2ZnO2+ H2O (अम्लीय व्यवहार)
प्रश्न 7.
दो धातुओं के नाम बताइए जो तनु अम्ल से हाइड्रोजन को विस्थापित कर देंगे तथा दो धातुएँ जो ऐसा नहीं कर सकती हैं। ..
उत्तर-
जिंक (Zn) एवं लोहा (Fe), हाइड्रोजन से अधिक अभिक्रियाशील होने के कारण उसे तनु अम्ल से विस्थापित कर सकते हैं। इसके विपरीत कॉपर (Cu) एवं पारा (Hg), हाइड्रोजन से कम अभिक्रियाशील होने के कारण ऐसा नहीं कर सकते।
प्रश्न 8.
किसी धातु M के विद्युत् अपघटनी परिष्करण में आप ऐनोड-कैथोड एवं विद्युत् अपघट्य किसे बनाएँगे?
उत्तर-
ऐनोड-धातु M की अशुद्ध मोटी प्लेट। कैथोड-शुद्ध धातु M की विद्युत् पतली प्लेट। विद्युत् अपघट्य-M धातु के यौगिक का जल में विलयन।
प्रश्न 9.
प्रत्यूष ने सल्फर चूर्ण को स्पैचुला में लेकर उसे गर्म किया। चित्र के अनुसार एक परखनली को उलटा कर के उसने उत्सर्जित गैस को एकत्र किया।
(a) गैस की क्रिया क्या होगी ?
(i) सूखे लिटमस पत्र पर
(ii) आर्द्र लिटमस पत्र पर।
(b) ऊपर की अभिक्रियाओं के लिए संतुलित रासायनिक अभिक्रिया लिखिए।
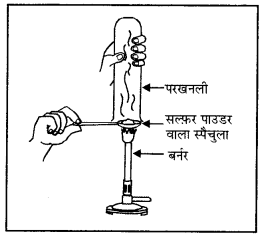
उत्तर-
(a) सल्फर जलने पर सल्फर डाइऑक्साइड उत्पन्न करता है।
S (s) + O2(g) → SO2 (g) सल्फर डाइऑक्साइड
- सूखे लिटमस पत्र पर गैस की कोई भी क्रिया नहीं होगी।
- गैस आर्द्र लिटमस पत्र में मौजूद जल के साथ अभिक्रिया कर सल्फ्यूरिक अम्ल उत्पन्न करेगी जो नीले लिटमस पत्र को लाल कर देगा।
(b) SO2(g) + H2O (l) → H2SO3 (aq) सल्फ्यूरस अम्ल
प्रश्न 10.
लोहे को जंग से बचाने के लिए दो तरीके बताइए।
उत्तर-
जंग से बचाने के.तरीके
1. तेल या ग्रीस की तह जमाकर-यदि लोहे पर तेल या ग्रीस की तह जमा दें तो नम वायु लोहे के संपर्क में नहीं आ पाती जिससे जंग नहीं लगता। मशीनों के पुर्जी को जंग से बचाने के लिए ऐसा ही किया जाता है।
2. एनेमल से-लोहे की सतह पर रंग-रोगन की तह जमाकर जंग लगने पर नियंत्रण पाया जाता है। बसों, कारों, स्कूटर-मोटर साइकिल, खिड़कियों, रेलगाड़ियों आदि पर एनेमल की परत जमाई जाती है।
प्रश्न 11.
ऑक्सीजन के साथ संयुक्त होकर अधातुएँ कैसा ऑक्साइड बनाती हैं ?
उत्तर-
अधातुएं, ऑक्सीजन से संयोग करके दो प्रकार के ऑक्साइड बनाती हैं।
(i) अम्लीय ऑक्साइड और
(ii) उदासीन ऑक्साइड।
(i) अम्लीय ऑक्साइड-अधातुएं, ऑक्सीजन से संयोग करके सह-संयोजक ऑक्साइड बनाती हैं जो पानी में घुलकर अम्ल बनाते हैं।
(a) C + O2 → CO2,
CO2 + H2O → H2CO3
कार्बोनिक अम्ल ।
(b) S + O2 → SO2
SO2 + H2O → H2SO3
(ii) उदासीन ऑक्साइड-कुछ अधातुएं, ऑक्सीजन से संयोग करके उदासीन ऑक्साइड बनाती हैं। इन का लिटमस पत्र पर कोई प्रभाव नहीं होता है जैसे-कार्बन मोनो-ऑक्साइड (CO), पानी (H2O) तथा नाइट्रस ऑक्साइड (N2O) उदासीन ऑक्साइड हैं।
प्रश्न 12.
कारण बताइए
(a) प्लैटिनम, सोना एवं चाँदी का उपयोग आभूषण बनाने के लिए किया जाता है।
(b) सोडियम, पोटैशियम एवं लीथियम को तेल के अंदर संग्रहीत किया जाता है।
(c) ऐलुमीनियम अत्यंत अभिक्रियाशील धातु है, फिर भी इसका उपयोग खाना बनाने वाले बर्तन बनाने के लिए किया जाता है।
(d) निष्कर्षण प्रक्रम में कार्बोनेट एवं सल्फाइड अयस्क को ऑक्साइड में परिवर्तित किया जाता है।
उत्तर-
(a) प्लैटिनम, सोना तथा चाँदी का प्रयोग आभूषण बनाने में किया जाता है क्योंकि ये धातुएँ सक्रियता श्रेणी में निम्नतम स्थान पर होती हैं तथा जल, ऑक्सीजन अथवा अम्लों से अभिक्रिया नहीं करतीं। ये धातुएँ संक्षारित नहीं होती तथा ये धातुएँ आघातवर्ध्यनीय तथा तन्य होती हैं। इसलिए इनसे आभूषणों के विभिन्न डिज़ाइन सरलतापूर्वक बनाए जा सकते हैं।
(b) सोडियम, पोटैशियम एवं लीथियम को तेल के अंदर संगृहित किया जाता है। इन्हें वायु के संपर्क में रखने पर आग पकड़ लेती हैं क्योंकि इन धातुओं का ज्वलन ताप (Ignition temperature) अत्यंत कम होता है। इसलिए इन्हें आग लगने से बचाने के लिए तेल के अंदर डुबोकर रखा जाता है।
(c) एल्यूमीनियम ताप की सुचालक है, परंतु यह अत्याधिक अभिक्रियाशील है। आई वायु के संपर्क में आने पर इसकी सतह पर पार न किए जाने वाली एल्यूमीनियम ऑक्साइड (Al2O3) की परत चढ़ जाती है। यह परत क्रियाशील धातु को अन्य पदार्थों के संपर्क में नहीं आने देती और धातु को जंग लगने से बचाती है। इन सभी कारणों से एल्यूमीनियम का प्रयोग खाना बनाने के बर्तन बनाने में किया जाता है।
(d) धातु कार्बोनेट और धातु सल्फाइड को धातु में बदलना कठिन होता है इसलिए इसे पहले धातु ऑक्साइड में बदलना आवश्यक होता है। अपचयन द्वारा इसे धातु ऑक्साइड में बदला जा सकता है। धातु कार्बोनेट को वायु की अनुपस्थिति में गर्म करके कार्बन डाइऑक्साइड को निष्कासित कर दिया जाता है।
![]()
धातु सल्फाइड को ऑक्सीजन की उपस्थिति में गर्म करके उसे धातु ऑक्साइड में रूपांतरित किया जाता है। इससे गंधक और आर्सेनिक जैसी अशुद्धियां भी दूर हो जाती हैं।
2ZnS + 3O2→ 2ZnO + 2SO2
S + O2→ SO2
4As + 5O2→ 2As2O5
प्रश्न 13.
आपने तांबे के मलीन बर्तन को नींबू या इमली के रस से साफ करते अवश्य देखा होगा। यह खट्टे पदार्थ बर्तन को साफ करने में क्यों प्रभावी हैं ?
उत्तर-
मलीन ताँबे के बर्तन पर जमी हुई कॉपर कार्बोनेट की परत नींबू या इमली के रस में उपस्थित अम्लों (सिटरिक अम्ल) से अभिक्रिया करके बर्तन से हट जाती है और बर्तन साफ हो जाता है। अत: खट्टे पदार्थ तांबे के बर्तन को साफ करने में प्रभावी होते हैं।
प्रश्न 14.
रासायनिक गुणधर्मों के आधार पर धातुओं एवं अधातुओं में विभेद कीजिए।
उत्तर-
रासायनिक गुणों के आधार पर धातुओं तथा अधातुओं में अंतर-
| धातु | अधातु |
| (1) धातुएँ क्षारीय ऑक्साइड बनाती हैं। | (1) अधातुएँ अम्लीय अथवा उदासीन ऑक्साइड बनाती हैं। |
| (2) धातुएँ तनु अम्लों से हाइड्रोजन विस्थापित इसलिए इनसे हाइड्रोजन विस्थापित नहीं करती है। | (2) अधातुएँ तनु अम्लों से अभिक्रिया नहीं करती कर देती हैं। |
| (3) धातुएँ क्लोरीन के साथ विद्युत् संयोजी क्लोराइड (आयनिक यौगिक) बनाती हैं। ये विद्युत् संयोजी क्लोराइड विद्युत्-अपघट्य, परंतु अवाष्पशील होते हैं। | (3) अधातुएँ क्लोरीन के साथ सहसंयोजी यौगिक बनाती हैं जो विद्युत्-अपघट्य, परंतु वाष्पशील होते हैं। |
| (4) धातुएँ अपचायक होती हैं। | (4) कार्बन को छोड़कर अधातुएँ ऑक्सीकारक होती हैं। |
| (5) धातुएँ हाइड्रोजन से संयोग करके हाइड्राइड बनाती हैं जो सहसंयोजक होते हैं। | (5) अधातुएँ हाइड्रोजन से क्रिया करके हाइड्राइड बनाती हैं। |
प्रश्न 15.
एक व्यक्ति प्रत्येक घर में सुनार बनकर जाता है। उसने पुराने एवं मलीन सोने के आभषणों में पहले जैसी चमक पैदा करने का ढोंग रचाया। कोई संदेह किए बिना ही एक महिला अपने सोने के कंगन उसे देती है जिसे वह एक विशेष विलयन में डाल देता है। कंगन नए की तरह चमकने लगते हैं लेकिन उनका वज़न अत्यंत कम हो जाता है। वह महिला बहुत दुःखी होती है तथा तर्क-वितर्क के पश्चात् उस व्यक्ति को झुकना पड़ता है। एक जासूस की तरह क्या आप उस विलयन की प्रकृति के बारे में बता सकते हैं ?
उत्तर-
सुनार द्वारा प्रयोग किया गया विलयन, एक्वारीजिया है। एक्वारीजिया विलयन में तनु हाइड्रोक्लोरिक अम्ल एवं नाइट्रिक अम्ल, 3 : 1 के अनुपात में होता है। सोना एक्वारीजिया में घुलनशील है इसलिए महिला के कंगन का भार कम हो जाता है।
प्रश्न 16.
गर्म जल का टैंक बनाने में तांबे का उपयोग होता है परंतु इस्पात (लोहे का मिश्रधातु) का नहीं। इसका कारण बताइए।
उत्तर-
कॉपर की उष्मा चालकता स्टील की अपेक्षा अधिक है। ऊर्जा बचाने के लिए गर्म पानी के टैंक को कॉपर से बनाया जाता है। कॉपर जल से अभिक्रिया भी नहीं करता भले उसे कितना भी गर्म किया जाए परंतु दूसरी ओर लोहा गर्म करने पर जल से क्रिया करता है।

Science Guide for Class 10 PSEB धातु एवं अधातु InText Questions and Answers
प्रश्न 1.
ऐसी धातु का उदाहरण दीजिए जो –
(i) कमरे के तापमान पर द्रव होती है।
(ii) चाकू से आसानी से काटा जा सकता है।
(iii) ऊष्मा की सबसे अच्छी चालक होती है।
(iv) ऊष्मा की कुचालक होती है।
उत्तर-
(i) पारा (Mercury)
(ii) सोडियम (Sodium)
(iii) चाँदी (Silver)
(iv) HRAT (Lead)
प्रश्न 2.
आघातवर्ध्य तथा तन्य का अर्थ बताइए।
उत्तर-
आघातवर्ध्य- धातुओं का वह गुणधर्म जिसके कारण धातुओं को हथौड़े से पीट-पीट कर बिना टूटे धातुओं को पतली चादरों में परिवर्तित किया जा सकता है। तन्य-धातुओं का वह गुणधर्म है जिस कारण उन्हें खींच कर पतली तारों में परिवर्तित किया जा सकता है।
प्रश्न 3.
सोडियम को किरोसिन तेल में डुबोकर क्यों रखा जाता है ?
अथवा
सोडियम तथा पोटाशियम को मिट्टी के तेल में डुबोकर क्यों रखा जाता है ?
उत्तर-
सोडियम तथा पोटाशियम को किरोसिन तेल में डुबोकर रखना-सोडियम एक अत्यंत सक्रिय धातु है जो वायु में रखने पर ऑक्सीजन से क्रिया करके सोडियम ऑक्साइड बनाती है तथा पानी के साथ क्रिया करके सोडियम हाइड्रोक्साइड तथा हाइड्रोजन गैस उत्पन्न करती है। हाइड्रोजन अत्यंत ज्वलनशील गैस है जिससे यह आग पकड़ लेती है। इसलिए सोडियम का वायु से संपर्क हटाने के लिए इसे किरोसिन तेल में डुबोकर रखा जाता है।
प्रश्न 4.
इन अभिक्रियाओं के लिए समीकरण लिखिए
(i) भाप के साथ आयरन,
(ii) जल के साथ कैल्शियम तथा पोटैशियम।
उत्तर-
(i) 3Fe (s) + 4H2O(g) → Fe3O4(s) + 4H2(g)
(ii) Ca(s) + 2H2O(l) → Ca (OH)2 (aq) + H2(g)
2K(s) + 2H2O(l) → 2KOH (aq) + H2(g)
प्रश्न 5.
A, B, C एवं D चार धातुओं के नमूनों को लेकर एक-एक करके निम्न विलयन में डाला गया। इससे प्राप्त परिणाम को निम्न प्रकार से सारणीबद्ध किया गया है :
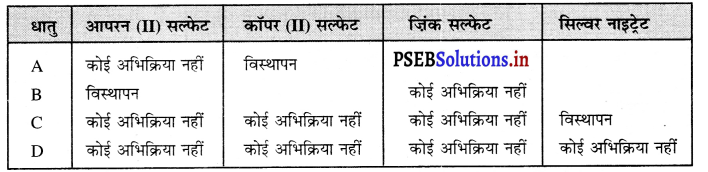
उत्तर-
(i) धातु ‘B’ सर्वाधिक अभिक्रियाशील है, क्योंकि कोई अन्य धातु FeSOA (आयरन सल्फेट) में से धातु को विस्थापित नहीं कर सकती।
(ii) धातु ‘B’ सर्वाधिक अभिक्रियाशील है। इसलिए यदि धातु को कॉपर (II) सल्फेट के विलयन में डाला जाए तो यह कॉपर को उसके विलयन से विस्थापित कर देगा और विलयन का नीला रंग फीका पड़ जाएगा।
(iii) B > A > C > D
प्रश्न 6.
अभिक्रियाशील धातु को तनु हाइड्रोक्लोरिक अम्ल में डाला जाता है तो कौन-सी गैस निकलती है ? आयरन के साथ तनु H,SO, की रासायनिक अभिक्रिया लिखिए।
उत्तर-
सभी धातुएँ तनु हाइड्रोक्लोरिक अम्ल से क्रिया नहीं करती हैं। केवल अभिक्रियाशील धातुएँ तनु हाइड्रोक्लोरिक अम्ल से क्रिया कर उसमें से हाइड्रोजन विस्थापित होकर गैस के रूप में उत्पन्न होती है। आयरन के साथ तनु सल्फ्यूरिक अम्ल (H2SO4) रासायनिक क्रिया से हाइड्रोजन गैस निकलती है।

प्रश्न 7.
जिंक को आयरन (II) सल्फेट के विलयन में डालने से क्या होता है ? इसकी रासायनिक अभिक्रिया लिखिए।
उत्तर-
जब ज़िंक को आयरन (II) सल्फेट के घोल में डाला जाता है तो जिंक आयरन सल्फेट के घोल से आयरन को विस्थापित कर देती है और आयरन सल्फेट का हरा रंग फीका पड़ जाता है। ऐसा इसलिए होता है कि जिंक आयरन की अपेक्षा अधिक अभिक्रियाशील है।
Zn + FeSO4 → ZnSO4 + Fe
इस क्रिया को इस प्रकार भी प्रदर्शित किया जा सकता है
Zn (s) → Zn2+ + 2e–
Fe2 (aq) + 2e– → Fe (s)
Fe2+ (aq) + Zn (s) → Zn2+ (aq) + Fe (s)
FeSO4 (aq) + Zn (s) → ZnSO4 (aq) + Fe (s).
प्रश्न 8.
(i) सोडियम, ऑक्सीजन एवं मैग्नीशियम के लिए इलेक्ट्रॉन-बिंदु संरचना लिखिए।
(ii) इलेक्ट्रॉन के स्थानांतरण के द्वारा Na2O एवं Mgo का निर्माण दर्शाइए।
(iii) इन यौगिकों में कौन-से आयन उपस्थित हैं ?
उत्तर-

(ii) इलेक्ट्रॉन स्थानांतरण द्वारा Na2O का निर्माण ।

इलेक्ट्रॉन स्थानांतरण द्वारा Mgo का निर्माण

(iii) Na2O में उपस्थित आयन
धनायन- Na+ (सोडियम धनायन)
ऋणायन- O2- (ऑक्सीजन ऋणायन)
Ma2O में उपस्थित आयन
धनायन- Mg2+ (सोडियम धनायन)
ऋणायन-O2- (ऑक्सीजन ऋणायन)
प्रश्न 9.
आयनिक यौगिकों का गलनांक उच्च क्यों होता है ?
उत्तर-
आयनिक यौगिकों के उच्च गलनांक-आयनिक यौगिकों के उच्च गलनांक होते हैं क्योंकि इन यौगिकों के आयनों के मध्य उपस्थित प्रबल अंतर-आयनिक आकर्षण बलों को समाप्त करने हेतु अधिक मात्रा में ऊर्जा की आवश्यकता पड़ती है। अतः इनका गलनांक उच्च होता है।
प्रश्न 10.
इन पदार्थों की परिभाषा दीजिए :
(i) खनिज
(ii) अयस्क
(iii) गैंग।
उत्तर-
(i) खनिज- धातुयुक्त पदार्थ जिनसे धातुएं विविध विधियों द्वारा प्राप्त की जाती हैं, को खनिज कहते हैं।
(ii) अयस्क- जिस खनिज से धातु, प्राप्त करना सरल तथा आर्थिक रूप से लाभदायक हो उसे अयस्क कहते हैं।
(iii) गैंग- पृथ्वी से निकाले गए अयस्कों के साथ अवांछनीय पदार्थ, गैंग कहलाते हैं।
प्रश्न 11.
दो धातुओं के नाम बताइए जो प्रकृति में मुक्त अवस्था में पाई जाती हैं।
उत्तर-
सोना (Au) एवं प्लैटिनम (Pt) प्रकृति में मुक्त अवस्था में पाई जाती हैं।
प्रश्न 12.
धातु को उसके ऑक्साइड से प्राप्त करने के लिए किस रासायनिक प्रक्रिया का प्रयोग किया जाता है?
उत्तर-
सक्रियता श्रेणी में निम्न स्थित धात्विक ऑक्साइडों को गर्म करने से धातु की प्राप्ति होती है, लेकिन सक्रियता श्रेणी के मध्य में स्थित धातुओं के ऑक्साइडों को कार्बन के साथ गर्म करके धातु प्राप्त की जाती है। इसे अपचयी क्रिया कहते हैं।
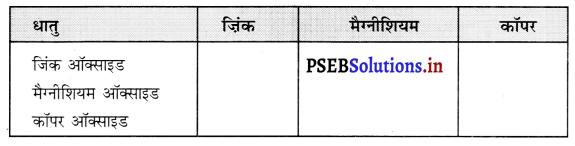
प्रश्न 13.
जिंक मैग्नीशियम एवं कॉपर के धात्विक ऑक्साइड को निम्न धातुओं के साथ गर्म किया गया :
उत्तर-
- ज़िंक ऑक्साइड तथा मैग्नीशियम में विस्थापन अभिक्रिया होगी।
ZnO + Mg → MgO + Zn - मैग्नीशियम ऑक्साइड विस्थापन अभिक्रिया नहीं कर सकता।
- कॉपर ऑक्साइड जिंक और मैग्नीशियम के साथ गर्म करने पर विस्थापन अभिक्रिया करेगा।
CuO + Zn → ZnO + Cu
CuO + Mg → MgO + Cu

प्रश्न 14.
कौन-सी धातु आसानी से संक्षारित नहीं होती है?
उत्तर-
वे धातुएँ जो वायु, जल तथा अम्लों से अभिक्रिया नहीं करतीं, शीघ्रता से संक्षारित नहीं होती; जैसेउत्कृष्ट धातुएँ, सोना, प्लैटिनम आदि।
प्रश्न 15.
मिश्रधातु क्या होते हैं ?
उत्तर-
मिश्रधातु-दो या दो से अधिक धातुओं के परस्पर मिलने से प्राप्त समांगी मिश्रण को मिश्र-धातु (alloy) कहते हैं। एक धातु व एक अधातु के समाँगी मिश्रण को भी मिश्रधातु कहते हैं। मिश्रातु के गुणधर्म मूल धातुओं से भिन्न होते हैं। शुद्ध धातु की अपेक्षा, मिश्रधातु की विद्युत् चालकता कम होती है।