Punjab State Board PSEB 10th Class Science Book Solutions Chapter 2 अम्ल, क्षारक एवं लवण Textbook Exercise Questions, and Answers.
PSEB Solutions for Class 10 Science Chapter 2 अम्ल, क्षारक एवं लवण
PSEB 10th Class Science Guide अम्ल, क्षारक एवं लवण Textbook Questions and Answers
प्रश्न 1.
कोई विलयन लाल लिटमस को नीला कर देता है, इसका pH संभवतः क्या होगा?
(a) 1
(b) 4
(c) 5
(d) 10.
उत्तर-
विलयन लाल लिटमस को नीला कर देता है इसलिए इसका pH अवश्य 7 से अधिक होना चाहिए। अतः
(d) ठीक उत्तर है।
प्रश्न 2.
कोई विलयन अंडे के पिसे हुए कवच से अभिक्रिया कर एक गैस उत्पन्न करता है जो चूने के पानी को दुधिया कर देता है। इस विलयन में क्या होगा?
(a) NaCl
(b) HCl
(c) LiCl
(d) KCl.
उत्तर-
अंडे के पिसे हुए कवच में CaCO, होता है जो HCI से क्रिया करके CO, उत्पन्न करता है जो चूने के पानी को दुधिया कर देती है।
ठीक उत्तर (b) होगा।
प्रश्न 3.
NaOH का 10ml विलयन, HCI के 8 ml विलयन में पूर्णतः उदासीन हो जाता है। यदि हम NaOH के उसी विलयन का 20ml लें तो इसे उदासीन करने के लिए HCI के उसी विलयन की कितनी मात्रा की आवश्यकता होगी?
(a) 4 ml
(b) 8 ml
(c) 12 ml
(d) 16 ml.
उत्तर-
यदि हम NaOH विलयन की दुगुनी मात्रा लेंगे ताकि HCI विलयन को उदासीन किया जा सके तो उसे भी दुगुना होना चाहिए।
अतः ठीक उत्तर (d) होगा।
![]()
प्रश्न 4.
अपच का उपचार करने के लिए निम्न में से किस औषधि का उपयोग होता है?
(a) एंटिबायोटिक (प्रतिजैविक)
(b) ऐनालजेसिक (पीड़ाहारी)
(c) एन्टैसिड
(d) ऐंटीसेप्टिक (प्रतिरोधी)।
उत्तर-
(c) एन्टैसिड।
प्रश्न 5.
निम्न अभिक्रिया के लिए पहले शब्द-समीकरण लिखिए तथा उसके बाद संतुलित समीकरण लिखिए
(a) तनु सल्फ्यूरिक अम्ल दानेदार जिंक के साथ अभिक्रिया करता है।
(b) तनु हाइड्रोक्लोरिक अम्ल मैग्नीशियम पट्टी के साथ अभिक्रिया करता है।
(c) तनु सल्फ्यूरिक अम्ल ऐलुमिनियम चूर्ण के साथ अभिक्रिया करता है।
(d) तनु हाइड्रोक्लोरिक अम्ल लौह के रेतन के साथ अभिक्रिया करता है।
उत्तर-
(a) जिंक + सल्फ्यूरिक अम्ल (तनु) → जिंक सल्फेट + हाइड्रोजन
Zn + H2SO4 → ZnSO + H2
(b) मैग्नीशियम + हाइड्रोक्लोरिक अम्ल → मैग्नीशियम क्लोराइड + हाइड्रोजन
Mg + 2HCI → MgCl2 + H2
(c) एलुमिनियम + सल्फ्यूरिक अम्ल → एलुमिनियम सल्फेट + हाइड्रोजन
2Al + 3H2 SO4 → Al2 (SO4)3 + 3H2
(d) लोहा + हाइड्रोक्लोरिक अम्ल → लोहा (II) क्लोराइड + हाइड्रोजन
Fe + 2HCl → FeCl + H2
प्रश्न 6.
ऐल्कोहॉल एवं ग्लूकोज़ जैसे यौगिकों में भी हाइड्रोजन होती है लेकिन इनका वर्गीकरण अम्ल की तरह नहीं होता है। एक क्रियाकलाप के द्वारा साबित कीजिए।
उत्तर-
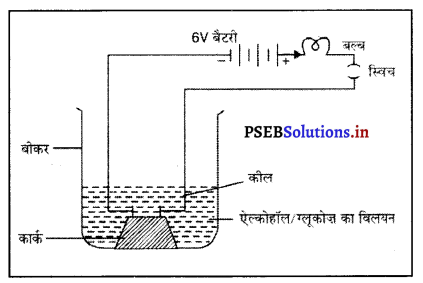
यद्यपि ऐल्कोहॉल एवं ग्लूकोज़ जैसे यौगिकों में हाइड्रोजन होती है पर वे बैटरी विलयन में आयनीकृत नहीं होते और H+ बल्ब आयन उत्पन्न नहीं करते। यह इस तथ्य से साबित होता है कि उनके विलयन विद्युत चालन नहीं करते।
क्रिया-कलाप–एक बीकर में ऐल्कोहॉल, ग्लूकोज़ आदि का विलयन लीजिए। कील एक कार्क पर दो कील लगाकर कॉर्क को ऐल्कोहॉल/ ग्लूकोज़ का विलयन बीकर में रख दीजिए। कीलों को 6 वोल्ट की कार्कएक बैटरी के दोनों टर्मिनलों के साथ एक बल्ब और स्विच के माध्यम से जोड़ दीजिए। अब विद्युत् धारा प्रवाहित कीजिए। विद्युत् चालन नहीं हुआ।
प्रश्न 7.
आसवित जल विद्युत् चालन क्यों नहीं होता जबकि वर्षा जल होता है?
उत्तर-
वर्षा जल में CO2, SO2, जैसी गैसें घुली होती हैं जो कार्बोनिक अम्ल (H2CO3), सल्फ्यूरस अम्ल (H2SO3) आदि बनाती है। इनका आयनों में विच्छेदन होता है। इसीलिए वर्षा जल में विद्युत् का चालन होता है। आसवित जल में घुलनशील लवण या गैसें नहीं होती इसलिए इसका आयनीकरण नहीं होता और इसमें विद्युत् का चालन नहीं होता।
प्रश्न 8.
जल की अनुपस्थिति में अम्ल का व्यवहार अम्लीय क्यों नहीं होता है ?
उत्तर-
जल किसी अम्ल के विच्छेदन में सहायक होता है जिससे हाइड्रोनियम (H3O+) आयन उत्पन्न होता है। जल की अनुपस्थिति में आयन उत्पन्न नहीं होते। इसलिए जल की अनुपस्थिति में अम्ल का व्यवहार अम्लीय नहीं होता।
![]()
प्रश्न 9.
पाँच विलयनों A, B, C, D व E की जब सार्वत्रिक सूचक से जाँच की जाती है तो pH के मान क्रमशः 4, 1, 11, 7 एवं 9 प्राप्त होते हैं। कौन-सा विलयन :
(a) उदासीन है?
(b) प्रबल क्षारीय है?
(c) प्रबल अम्लीय है?
(d) दुर्बल अम्लीय है?
(e) दुर्बल क्षारीय है?
pH के मानों को हाइड्रोजन आयन की सांद्रता के आरोही क्रम में व्यवस्थित कीजिए।
उत्तर-
दिए गए pH के मान हैं-A = 4, B = 1, C = 11, D = 7, E = 9.
(a) जब pH = 7 हो तो विलयन उदासीन होता है।
∴ D उदासीन विलयन है।
(b) 7 से जितना अधिक pH का मान होगा विलयन उतना ही अधिक क्षारीय होगा।
∴C प्रबल क्षारीय होगा।
(c) 7 से जितना कम pH का मान होगा विलयन उतना ही अम्लीय होगा।
∴ B प्रबल अम्लीय होगा।
(d) 7 से कम लेकिन 7 के निकट दुर्बल अम्लीय होगा
∴ A दुर्बल अम्लीय है।
(e) 7 से अधिक लेकिन 7 के निकट दुर्बल क्षारीय होगा।
∴ E दुर्बल क्षारीय है।
दिए हुए विलयनों की हाइड्रोजन आयन सांद्रता होगी
A = 10-4 M. B = 10-1 M, C = 10-11M
D = 10-7M. E = 10-9M
∴ आरोही क्रम में व्यवस्था = C (10-11M) < E (10-9 M) < D (10-7M) -1M) < B(10-1 M)
प्रश्न 10.
परखनली ‘A’ एवं ‘B’ में समान लंबाई की मैग्नीशियम की पट्टी लीजिए। परखनली ‘A’ में हाइड्रोक्लोरिक अम्ल (HCI) तथा परखनली ‘B’ में ऐसीटिक अम्ल (CH3COOH) डालिए। दोनों अम्लों की मात्रा तथा सांद्रता समान है। किस परखनली में अधिक तेजी से बुदबुदाहट होगी और क्यों?
उत्तर-
परखनली ‘A’ में अधिक तेज़ी से बुदबुदाहट होगी। ऐसा इसलिए कि हाइड्रोक्लोरिक अम्ल ऐसीटिक अम्ल से प्रबल है। मैग्नीशियम की क्रिया हाइड्रोक्लोरिक अम्ल से तीव्र होगी और हाइड्रोजन गैस उत्पन्न होगी।
प्रश्न 11.
ताजे दूध के pH का मान 6 होता है। दही बन जाने पर इसके pH के मान में क्या परिवर्तन होगा? अपना उत्तर समझाइए।
उत्तर-
जब ताज़ा दूध दही में बदल जाता है तो pH कम हो जाएगा। ऐसा इसलिए होगा कि दही अधिक अम्लीय होता है। दही में लैक्टिक अम्ल होता है। जितना अधिक अम्ल होगा उसका pH उतना ही कम होगा।
प्रश्न 12.
एक ग्वाला ताजे दूध में थोड़ा बेकिंग सोडा मिलाता है।
(a) ताज़ा दूध के pH के मान को 6 से बदल कर थोड़ा क्षारीय क्यों बना देता है?
(b) इस दूध को दही बनने में अधिक समय क्यों लगता है ?
उत्तर-
(a) ताज़ा दूध अम्लीय है और खट्टा होकर अधिक अम्लीय हो जाता है। बेकिंग सोडा की उपस्थिति में दूध क्षारीय हो जाएगा और जल्दी से खट्टा नहीं होगा क्योंकि क्षार दूध को शीघ्रता से अम्लीय बनने से रोक देगा।
(b) जब दूध दही में बदलता है तो लैक्टिक अम्ल बनने के कारण उसका pH कम हो जाता है। क्षार की उपस्थिति इसे जल्दी से अधिक अम्लीय होने से रोकती है इसलिए दूध को दही बनने में अधिक समय लगता है।
प्रश्न 13.
प्लास्टर ऑफ पेरिस को आर्द्र-रोधी बर्तन में क्यों रखा जाना चाहिए? इसकी व्याख्या कीजिए।
उत्तर-
प्लास्टर ऑफ पेरिस CaSO4 \(\frac{1}{2}\) H2O है। नमी की उपस्थिति के कारण यह जिप्सम बन जाता है।
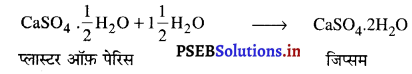
इसलिए इसे आर्द्र-रोधी बर्तन में रखा जाना चाहिए।
प्रश्न 14.
उदासीनीकरण अभिक्रिया क्या है ? दो उदाहरण दीजिए।
उत्तर-
उदासीनीकरण-जब अम्ल किसी क्षार से क्रिया करता है तब लवण और जल बनता है। इसे उदासीनीकरण अभिक्रिया कहते हैं।
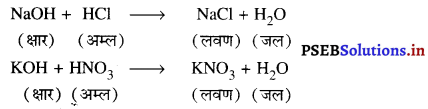
प्रश्न 15.
धोने का सोडा एवं बेकिंग सोडा के दो-दो प्रमुख उपयोग बताइए।
उत्तर-
(क) धोने का सोडा (Na2CO3.10H2O)
- इसका उपयोग कांच, साबुन और कागज़ उद्योगों में होता है।
- जल की स्थाई कठोरता को दूर करने के लिए इसका उपयोग होता है।
(ख) बेकिंग सोडा (NaHCO3)
- इसका प्रयोग सोडा-अम्ल अग्निशामक में किया जाता है।
- यह ऐंटैसिड का एक संघटक है जो पेट के अम्ल की अधिकता को उदासीन करके राहत पहुंचाता है।
Science Guide for Class 10 PSEB अम्ल, क्षारक एवं लवण InText Questions and Answers
प्रश्न-
आपको तीन परखनलियां दी गई हैं। इनमें से एक में आसवित जल एवं शेष दो में से एक में अम्लीय विलयन तथा दूसरे में क्षारीय विलयन है। यदि आपको केवल लाल लिटमस पत्र दिया जाता है तो आप प्रत्येक परखनली में रखे गए पदार्थों की पहचान कैसे करेंगे?
उत्तर-
तीनों परखनलियों में लाल लिटमस पत्र को डुबाओ। जिस परखनली में इसका रंग नीला हो जाएगा वह क्षारीय विलयन होगा। जिन अन्य दो परखनलियों में रंग परिवर्तन नहीं होगा उनमें जल और अम्लीय विलयन होगा। अब इसी लिटमस पत्र को, जो क्षारीय विलयन में डालने से नीला हो चुका है, उसे जल और अम्लीय विलयन में डालो। जिस परखनली में रंग में कोई परिवर्तन नहीं होगा उसमें जल होगा पर जिस परखनली में अम्लीय विलयन होगा उसमें नीले लिटमस का रंग पुनः लाल हो जाएगा।
प्रश्न 1.
पीतल एवं तांबे के बर्तनों में दही एवं खट्टे पदार्थ क्यों नहीं रखने चाहिए ?
उत्तर-
यदि पीतल तथा तांबे के बर्तनों में खट्टे पदार्थ रखे जाएंगे तो दही एवं खट्टे पदार्थ में मौजूद अम्ल पीतल तथा तांबे के साथ क्रिया करके विषैले यौगिक का निर्माण करेंगे जो हमारे शरीर के लिए हानिकारक हैं। इसलिए दही जैसे खट्टे पदार्थ को पीतल तथा तांबे के बर्तनों में नहीं रखना चाहिए।
प्रश्न 2.
धातु के साथ अम्ल की अभिक्रिया होने पर सामान्यत: कौन-सी गैस निकलती है? एक उदाहरण के द्वारा समझाइए। इस गैस की उपस्थिति की जाँच आप कैसे करेंगे?
उत्तर-
जब धातु के साथ अम्ल अभिक्रिया करते हैं तब प्रायः हाइड्रोजन गैस उत्पन्न होती है।
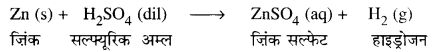
हाइड्रोजन गैस को साबुन के घोल से गुज़ारो। बुलबुले उत्पन्न होंगे। उन बुलबुलों के निकट जलती हुई मोमबत्ती की ज्वाला लाओ। वे फट-फट की ध्वनि के साथ जलेंगे। इस से हाइड्रोजन गैस की उपस्थिति सिद्ध हो जाती है।
![]()
प्रश्न 3.
कोई धातु यौगिक ‘A’ तनु हाइड्रोक्लोरिक अम्ल के साथ अभिक्रिया करता है तो बुदबुदाहट उत्पन्न होती है। इससे उत्पन्न गैस जलती मोमबत्ती को बुझा देती है। यदि उत्पन्न यौगिकों में एक कैल्सियम क्लोराइड है, तो इस अभिक्रिया के लिए संतुलित रासायनिक समीकरण लिखिए। उत्तर- इस अभिक्रिया के लिए संतुलित रासायनिक समीकरण है-

यौगिक ‘A’ अवश्य ही कैल्सियम कार्बोनेट है। यह तुन हाइड्रोक्लोरिक अम्ल से क्रिया कर कैल्सियम क्लोराइड, जल और कार्बन डाइऑक्साइड बनाता है। कार्बन डाइऑक्साइड में आग बुझाने का गुण होता है। इसीलिए वह जलती मोमबत्ती को बुझा देती है।
प्रश्न 4.
HCI, HNO, आदि जलीय विलयन में अम्लीय अभिलक्षण क्यों प्रदर्शित करते हैं, जबकि ऐल्कोहॉल एवं ग्लूकोज़ जैसे यौगिकों के विलयनों में अम्लीयता के अभिलक्षण नहीं प्रदर्शित होते हैं?
उत्तर-
HCI, HNO, आदि जलीय विलयन में अम्लीय अभिलक्षण प्रदर्शित करते हैं, क्योंकि ये जलीय विलयन में आयनीकरण कर के H+ आयन उत्पन्न करते हैं। जबकि ऐल्कोहॉल एवं ग्लूकोज़ आयनीकरण नहीं करते और विद्युत् H+ आयन को उत्पन्न नहीं करते। ये जलीय विलयन में विद्युत् चालकता का गुण प्रदर्शित नहीं करते। इसलिए ये अम्लीयता के अभिलक्षण प्रदर्शित नहीं करते हैं।
प्रश्न 5.
अम्ल का जलीय विलयन क्यों विद्युत् का चालन करता है?
उत्तर-
अम्ल का जलीय विलयन विद्युत् का चालन करता है क्योंकि यह जलीय विलयन में आयनीकरण कर के आयन उत्पन्न करता है।
HCl (aq) →HO(aq) + Cl- (aq)
HNO3 (aq) → HO+ (aq) + NO3 (aq)
प्रश्न 6.
शुष्क हाइड्रोक्लोरिक गैस शुष्क लिटमस पत्र का रंग क्यों नहीं बदलती है?
उत्तर-
शुष्क हाइड्रोक्लोरिक गैस शुष्क लिटमस पत्र का रंग नहीं बदलती क्योंकि जल की अनुपस्थिति में यह आयनीकरण न कर पाने के कारण H+ आयन उत्पन्न नहीं कर पाती। इस कारण वह अम्ल की तरह काम नहीं कर पाती।
प्रश्न 7.
अम्ल को तनुकृत करते समय यह क्यों अनुशंसित करते हैं कि अम्ल को जल में मिलाना चाहिए न कि जल को अम्ल में?
उत्तर-
जल में अम्ल के घुलने की प्रक्रिया अत्यंत ऊष्माक्षेपी होती है। इसलिए जल में किसी सांद्र अम्ल को सावधानीपूर्वक मिलाना चाहिए। अम्ल और जल को धीरे-धीरे हिलाते रहना चाहिए। ऐसा न करने पर अम्ल में जल मिलाने पर उत्पन्न ऊष्मा के कारण मिश्रण आस्फलित हो कर बाहर आ सकता है। इससे स्थानीय ताप बढ़ जाता है जिस कारण उपयोग किया जाने वाला कांच का पात्र टूट भी सकता है।
प्रश्न 8.
अम्ल के विलयन को तनुकृत करते समय हाइड्रोनियम आयन (H3O+) की सांद्रता कैसे प्रभावित हो जाती है?
उत्तर-
जल में अम्ल के विलयन को तनुकृत करते समय आयन की सांद्रता (H3O+/H+) में प्रति इकाई आयतन की कमी हो जाती है और विलयन तनु से अधिक तनु हो जाता है।
प्रश्न 9.
जब सोडियम हाइड्रॉक्साइड विलयन में आधिक्य क्षारक मिलाते हैं तो हाइड्रॉक्साइड आयन (OH–) की सांद्रता कैसे प्रभावित होती है ?
उत्तर-
जब सोडियम हाइड्रॉक्साइड विलयन में आधिक्य क्षारक मिलाते हैं तो हाइड्रॉक्साइड आयन (OH–)) की सांद्रता प्रति इकाई आयतन बढ़ती जाती है।
प्रश्न 10.
आपके पास दो विलयन ‘A’ एवं ‘B’ है। विलयन ‘A’ के pH का मान 6 है एवं विलयन ‘B’ के pH का मान 8 है। किस विलयन में हाइड्रोजन आयन की सांद्रता अधिक है ? इनमें से कौन अम्लीय है तथा कौन क्षारकीय?
उत्तर-
विलयन ‘A’ की हाइड्रोजन आयन सांद्रता विलयन ‘B’ की अपेक्षा अधिक है। विलयन A का pH मान 7 से कम है इसलिए वह अम्लीय है। विलयन B का pH मान 7 से अधिक है। इसलिए वह क्षारकीय है।
प्रश्न 11.
H+(aq) आयन की सांद्रता का विलयन की प्रकृति पर क्या प्रभाव पड़ता है ?
उत्तर-
H+(aq) आयन की सांद्रता का विलयन की प्रकृति पर प्रभाव पड़ता है। H+(aq) की जितनी सांद्रता होगी, उतना ही विलयन अधिक अम्लीय होगा।
![]()
प्रश्न 12.
क्या क्षारकीय विलयन में H+(aq) आयन होते हैं ? अगर हाँ, तो यह क्षारकीय क्यों होते हैं?
उत्तर-
क्षारकीय विलयन में H+ (aq) आयन होते हैं पर साथ ही उसमें OH– आयन भी होते हैं। वे क्षारकीय इसलिए होते हैं क्योंकि उनमें OH– आयन की सांद्रता अधिक H+ आयन की अपेक्षा अधिक होती है।
प्रश्न 13.
कोई किसान खेत की मृदा की किस परिस्थिति में बिना बुझा हुआ चूना (कैल्सियम ऑक्साइड) बुझा हुआ चूना (कैल्सियम हाइड्रॉक्साइड) या चॉक (कैल्सियम कार्बोनेट) का उपयोग करेगा?
उत्तर-
बिना बुझा हुआ चूना (CaO), बुझा हुआ चूना [Ca (OH)2] और चॉक (CaCO3) में प्रकृति से क्षारकीय है इसलिए किसान खेत की मृदा में इन का उपयोग कर सकेगा यदि उस खेत की प्रकृति अम्लीय है।
प्रश्न 14.
CaOCl2 यौगिक का प्रचलित नाम क्या है?
उत्तर-
विरंजक चूर्ण (Bleaching Powder)।
प्रश्न 15.
उस पदार्थ का नाम बताइए जो क्लोरीन से क्रिया करके विरंजक चूर्ण बनाता है?
उत्तर-
शुष्क बुझा हुआ चूना Ca (OH)2.
प्रश्न 16.
कठोर जल को मृदु करने के लिए किस सोडियम यौगिक का उपयोग किया जाता है ?
उत्तर-
धावन सोडा (Na2CO3)।
प्रश्न 17.
सोडियम हाइड्रोजनकार्बोनेट के विलयन को गर्म करने पर क्या होगा? इस अभिक्रिया के लिए समीकरण लिखिए।
उत्तर-
सोडियम हाइड्रोजन कार्बोनेट गर्म करने पर सोडियम कार्बोनेट कार्बन डाइऑक्साइड और जल में विघटित हो जाएगा।
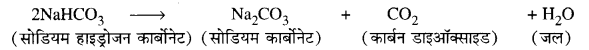
प्रश्न 18.
प्लास्टर ऑफ़ पेरिस की जल के साथ अभिक्रिया के लिए समीकरण लिखिए।
उत्तर-
प्लास्टर ऑफ़ पेरिस (CasO4 . \(\frac{1}{2}\) H2O) जल के साथ अभिक्रिया करके जिप्सम (CaSO4.2H2O) बनाता है और लगभग आधे घंटे में जम कर ठोस बन जाता है।